早期的疼痛管理与抗炎治疗在骨关节炎(OA)疾病管理中的价值
近年来诸多研究证据显示,慢性、低度炎症在OA的疼痛进展和病理结构改变中发挥了重要作用,而抗炎治疗,尤其是早期的OA抗炎治疗,对OA的疼痛和病程管理又有哪些益处?本篇文章将围绕”炎症在OA病理改变中的核心作用、炎症与OA痛觉敏化的关系、早期抗炎治疗对OA疾病管理的重要性”三个话题进行深入探讨。
炎症在OA病理改变中的核心作用
早在2013年,Jeremy Sokolove等人已就“炎症在OA病理改变中的作用——最新发现和解释”在“Therapeutic Advances in Musculoskeletal Disease” 上发表了综述,2016年该专家小组再次就“低度炎症是OA病理改变的关键因素”在Nature Reviews Rheumatology上进行了综述进展更新。其中提出了如下主要观点:
OA主要与高龄、关节创伤、生物力学改变、肥胖等多种危险因素相关。由于其病因的复杂性,OA不应被视为一种单一的疾病,而应被视作由多种失衡状态所导致的全身一个或多个关节完全破坏。
OA的病理改变共享了一个最终共同通路,导致了关节的持续性和完全性破坏(见图1):
-
由软骨损伤所激活的固有免疫(非特异性免疫)反应,在OA的启动和进展中发挥着关键的作用,并可能导致了随后滑膜炎的产生。
-
局部组织损伤和免疫系统之间的相互作用,导致了慢性、低度关节炎症状态,并最终导致临床OA的各种表现。
图1. 局部组织损伤与细胞、炎症、病理结构破坏之间相互作用的恶性循环2
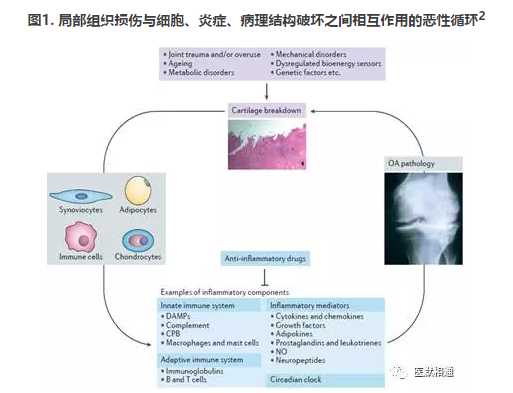
引自 William H. Robinson, et al. Nature Reviews Rheumatology; 2016, Vol.12: 580-592.
OA中的炎症通常被认为是由免疫应答参与的慢性、低度炎症,从根本上不同于类风湿性关节炎的高度炎症,而且参与的细胞和分子也不同(见图2)。 而在OA患者身上,使用治疗RA的生物疗法,全身性抑制传统炎症细胞因子的活性,并无获益,在侵袭性OA患者身上,也同样没有或仅有很少获益。
总之,系列证据证明,OA中的炎症机制不同于RA,需要新的抗炎治疗方案。
图2. 比较OA和RA患者血清和滑液样本中细胞因子的水平、健康个体血清样本中细胞因子的水平(细胞因子水平通过multiplex bead-based immunoassay 方法进行检测)1
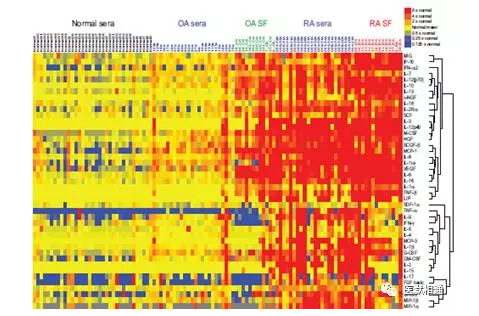
引自 Jeremy Sokolove,et al.Ther Adv Musculoskel Dis (2013) :5(2) 77–94 .
OA发病机制中的危险因素、细胞类型、炎症通路中的分子组成,均可作为预防和治疗OA的潜在治疗目标2(见图1) 。目前没有药物显示有改变OA结构破坏进展的效果。而现有治疗药物(包括传统NSAIDs药物、COX-2抑制剂、关节腔内注射透明质酸、糖皮质激素),都只能缓解OA疾病的症状1。
现有影像学技术和生物标志物的发展方向应定位于,方便检测现有治疗方案在OA进程早期的抗炎干预(此时治疗效果最佳),通过更早的诊断和更好的筛选病人更早、更准确的评估新药的临床治疗效果2。
炎症与OA痛觉敏化的关系
2016年Tuhina Neogi等人通过NIH资助的多中心OA研究(MOST),就“膝部OA的关节炎症与痛觉敏化的关系”在ARTHRITIS & RHEUMATOLOGY杂志发表了研究。
结果显示,滑膜炎可增加外周痛觉敏化,滑膜积液可增加中枢痛觉敏化。提示,炎症具有促进痛觉敏化进展和扩大的特点。并且,探索性分析中发现,持续性的滑膜炎和持续性的滑膜积液,与痛觉敏化随时间增强有关,即使祛除炎性刺激,可能也不足以改变疼痛的高敏状态3。
既然痛觉敏化与膝OA的疼痛严重性相关,并可导致急性疼痛转化为慢性持续性疼痛,那么说明,预防痛觉敏化的进展,可作为一种预防膝OA疼痛恶化的有效且新颖的方法。因此,在膝OA的早期进行抗炎治疗,可作为一种合理预防疼痛敏化的策略,并可由此减轻疼痛的严重程度3。
早期抗炎治疗/疼痛管理对OA疾病管理的重要性
OA治疗的早期应答可以预测总体疗效。研究显示,使用NSAIDs在治疗2周,有应答的OA患者中,绝大多数在12周时仍然有应答,表明应答状态在治疗初始2周时已经大致确定,而早期确定患者对NSAIDs药物的治疗反应,可以使得临床医生更有效的管理症状性OA5。
在OA的疼痛状态下,无论是外周神经还是脊髓神经的COX-2表达都是上调的。且使用NSAIDs的OA患者,脑脊液中COX-2抑制剂的水平与用药后疼痛的改善程度密切相关。由此可见,NSAIDs有双重的作用位点,可同时抑制外周和中枢水平的痛觉敏化6(见图3) 。已有研究证实,使用依托考昔60mg治疗疼痛性膝OA,可同时显著改善外周和中枢的痛觉敏化,并显著改善患者的疼痛和功能7。
图3. OA镇痛药物的外周和中枢作用位点6
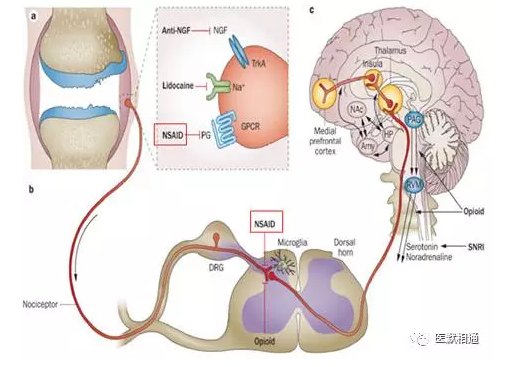
引自Anne-Marie Malfait,et al. Nature Reviews Rheumatology; 2013, 9(11): 654-664.
POWER研究(真实世界多中心临床研究)评价了传统NSAIDs、其他COX-2抑制剂、对乙酰氨基酚等治疗疗效欠佳的OA患者,换用依托考昔治疗4周后的疗效改善情况,结果显示:在所有疗效欠佳的患者中,换用依托考昔治疗4周后,有52%的WOMAC平地行走疼痛评分改善≥30%;其中基线时疼痛强度≥40mm的患者中,有66%的WOMAC平地行走疼痛评分改善≥30%;且显著改善了患者的日常活动与健康状态评估及研究者对治疗反应的总体评价等,并显著减少了胃肠道保护性药物的使用和胃肠道不适症状8。
目前研究显示,Cox-2抑制剂在OA患者(动物和人体)的不同组织中有着不同影响: 在软骨中,Cox-2抑制剂可以增加蛋白多糖的含量,同时对于多种炎症因子和软骨破坏的进程有着抑制作用。在滑膜组织中,Cox-2抑制剂表现出抑制炎症因子和滑膜巨噬细胞数量的效果。在骨组织中,Cox-2抑制剂可以增加小梁骨容量,并抑制软骨下骨骨吸收和破骨细胞的数量9。
图4. Cox-2抑制剂对OA患者软骨、滑膜、骨组织的影响9
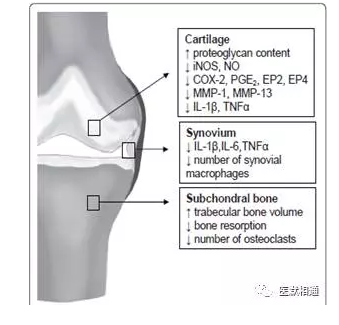
(COX, cyclooxygenase; iNOS, induciblenitric oxide synthase; MMP, matrixmetalloproteinase; NO, nitric oxide; PGE2,prostaglandin E2.)
Manon C Zweers,et al. Arthritis Research & Therapy; 2011,13(239): 1-11.
如前文所述,OA是一种炎性疾病,其慢性、低度炎症是导致OA疾病进展的主要原因。而这种炎症对外周和中枢感受器的痛觉敏化又是导致OA疼痛的直接原因。早期开始OA抗炎治疗,不仅可以潜在改善OA病程进展,还可以尽早缓解OA疼痛,改善患者生活质量,恢复运动功能减轻致残率。
在OA早期,尽早启用可透过血脑屏障的NSAIDs药物(如依托考昔)治疗OA,利用其外周和中枢的双重抗炎机制,可有效缓解骨关节的疼痛,并能防止急性疼痛转化为难治性慢性疼痛,更好的改善OA患者生活质量及运动功能。同时,Cox-2抑制剂的抗炎作用,也展现出改善OA疾病病程的潜在特点,未来可通过更规范的体内研究设计在该方面的作用进行进一步深入探索。
参考文献:
1. JeremySokolove,ChristinM.Lepus;Role of inflammation in the pathogenesis of osteoarthritis:latest findings and interpretations; TherAdvMusculoskelDis(2013)5(2)77–94;
2. William H. Robinson; JeremySokolove,etal;Low-grade inflammation as a key mediatorof the pathogenesis of osteoarthritis;NatureReviewsRheumatology;October 2016, Vol.12: 580-592;
3. Tuhina Neogi, Ali Guermazi,etal,; Association of Joint Inflammation WithPain Sensitization in Knee Osteoarthritis; Arthritis& Rheumatology; March2016, Vol.68(3):654–661
4. Dorothy D Dunlop , Jing Song , et al.; Relationofphysicalactivitytimetoincidentdisabilityincommunitydwellingadultswithoratriskofkneearthritis:prospectivecohortstudy.BMJ,2014,348(2472):1-11.
5. Clifton O. Bingham III, Steven S. Smugar, et al.; Early response to COX-2inhibitors as a predictor of overall response in osteoarthritis: pooled resultsfrom two identical trials comparing etoricoxib, celecoxib and placebo; Rheumatology; 2009, 48: 1122–1127.
6. Anne-Marie Malfait, Thomas J. Schnitzer; Towards a mechanism-basedapproach to pain management in osteoarthritis; NatureReviewsRheumatology; November 2013, 9(11): 654-664
7. L.Arendt-Nielsen, Line Lindhardt Egsgaard,etal.; Evidence for a central mode ofaction for Etoricoxib (COX-2 inhibitor) in patients with painful kneeosteoarthritis; Pain,August 2016,157: 1634–1644
8. Hsiao-Yi LIN,Tien-Tsai CHENG,et al.; Etoricoxibimprovespain,functionandqualityoflife: resultsofareal-worldeffectivenesstrial;InternationalJournalofRheumaticDiseases;2010, 13:144–150
9. ManonC Zweers, Tineke N de Boer,etal.; Celecoxib: considerations regarding its potential disease-modifyingproperties in osteoarthritis; ArthritisResearch&Therapy; 2011,13(239): 1-11
本文来源于医默相通,作者孙铁铮 北京大学人民医院关节病诊疗研究中心主任医师、教授,博士研究生导师,医学博士。从事关节疾病的外科治疗(包括微创治疗)和运动医学专业。
感谢您的关心与支持






